研究業績・内容
先天性フォン・ヴィレブランド病 (von Willebrand Disease:VWD)
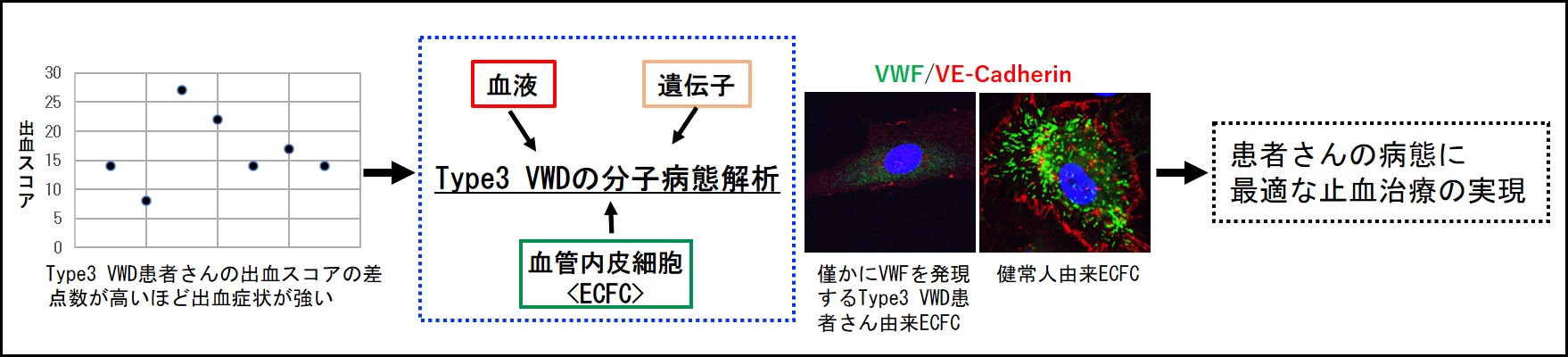
von Willebrand病 (VWD)では、von Willebrand因子 (VWF)の量的・質的異常によって止血障害を来します。最重症型のType3 VWDは、「VWFの完全欠損型」ですが、その出血症状の程度には幅があり、あまり出血しない患者さんもいます。患者さん毎に最適な止血治療を提供するためには「出血症状の幅」をもたらす原因を明らかにする必要があります。我々は、その原因を解明するために、Type3 VWDの分子病態解析を独自にセットアップしています。病因遺伝子の解析、VWF抗原量・活性値測定、multimer解析に加え、endothelial colony forming cell (ECFC)による血管内皮レベルでのVWF発現を評価し、より詳細な病態の解明を目指します。その成果として、臨床検査においてType3 VWDと診断された症例の中には、「微量のVWFを発現する亜型」が存在し、出血症状が比較的軽度であることを見出しました(Okamoto S et al.J.Thromb Haemost 2022)。
血友病
当研究グループは血友病の遺伝子解析を実施する国内でも数少ない研究組織です。血友病の責任遺伝子バリアントには複雑なものも多く、近年、広く行われるようになった次世代シークエンスでは同定できないものもあります。当研究グループでは一人一人の患者さんの遺伝子を手作業で丁寧に解析することにより、従来の手法では同定できなかった遺伝子バリアントも数多く明らかにしています。また凝固一段法と合成基質法による多角的な凝固因子活性測定に加え、Rotational thromboelastometry (ROTEM)やトロンビン生成試験(Thrombin generation assay:TGA)による包括的な血液凝固能検査を組み合わせて評価することにより、血友病の血液凝固能異常の特徴に迫ります。そして実際の出血頻度や関節症の進行度と照らし合わせて評価することにより、臨床症状に与えるインパクトについて検討し、より効果的な血友病治療の提案を目指します。その他、数々の治験や多施設共同研究に参加、主導しており、基礎・臨床両面から血友病研究を押し進めています。
Tokoro M et al. MGGM. 2020, Ogawa M et al. Thromb Res. 2020, Odaira K et al. Thromb Res. 2022, Matsushita T et al. BMJ Open. 2022. など
先天性血栓性疾患(血栓性素因)
2017年に成人の先天性血栓性疾患は「特発性血栓症」として指定難病に登録されました。この申請には病態責任遺伝子のバリアントを記入する欄が設けられており、日常診療においても、血栓性素因の遺伝子解析の重要性は増してきています。これまでに我々はアンチトロンビン欠乏症、プロテインC欠乏症、プロテインS欠乏症、さらには当研究グループが世界に先駆けて発見したアンチトロンビン抵抗性プロトロンビン異常症(ATR-FII)などの多種多様な先天性血栓性疾患の遺伝子解析および分子病態解析を行い、多数の報告を行ってきました。現在は血液を使った凝固能検査も確立することにより、一般病院などでは実施していないATR-FIIや活性化プロテインC抵抗性(Activated proteinC resistance:APCR)の検査も実施できる体制を整えています。
関連論文:Miyawaki Y et al. N Engl J Med. 2012, Tamura S et al. Thromb Res. 2019. Okada K et al. Thromb Res. 2022. など
フィブリノゲン検査法の創出
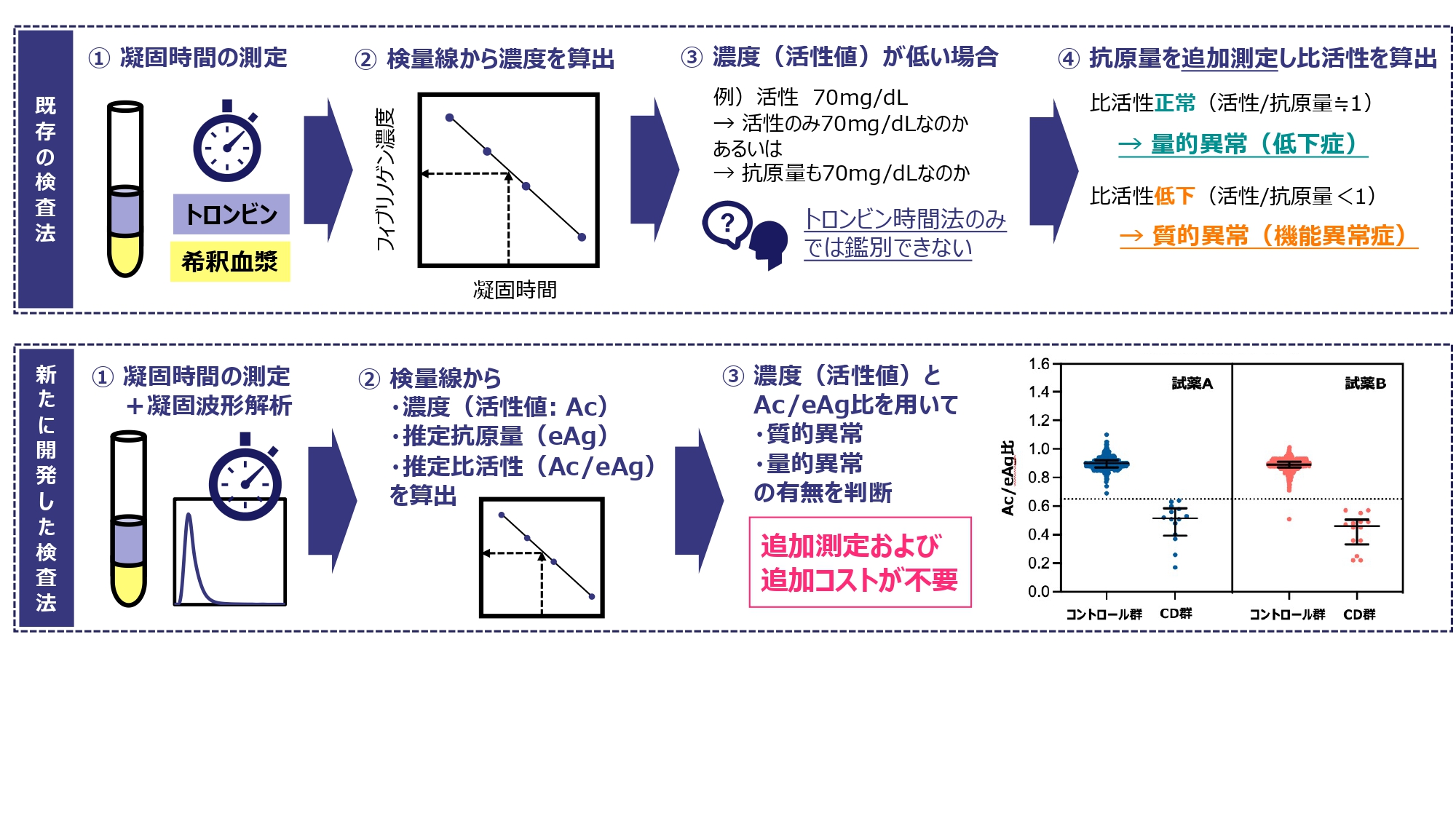
血液凝固反応の最終段階を担うフィブリノゲンの測定は血液凝固検査の中でも重要項目の一つです。フィブリノゲンの測定法は、そのほとんどがClauss法(トロンビン時間法)と呼ばれる方法です。しかし、この方法で評価することができるものは機能的なフィブリノゲン量(フィブリンへと転化することができるいわば活性値)で、その絶対的な量(抗原量)を捉えるものではありません。フィブリノゲンの異常には「量的異常」である低フィブリノゲン血症と「質的異常」である異常フィブリノゲン血症が存在しますが、どちらもClauss法では「フィブリノゲン低下症」にみえるためこれらを区別することはできません。これらの鑑別には免疫学的手法によりフィブリノゲン抗原量を測定し、活性値と抗原量の間に乖離があるかどうかを検証する必要があります。低フィブリノゲン血症と異常フィブリノゲン血症では出血症状などの臨床症状に大きな違いがあるため、この鑑別は非常に重要です。
名古屋大学医学部附属病院では、研究検査としてフィブリノゲン抗原量測定を実施できる体制を2017年に整備しました。また、最近では、凝固波形解析(Clot Waveform Analysis: CWA)技術を用いて新たなフィブリノゲンの質的分析法(Clauss-CWA法)の開発に成功しています。これはフィブリノゲン抗原量測定を必要とせず、Clauss法単独でフィブリノゲン異常症を鑑別できる追加コストが不要な画期的な手法です。また、Clauss-CWA法は世界初となるCWAの臨床応用であり、この最新技術を用いて現在様々な研究への展開を予定しています。
文献:鈴木敦夫ほか,日本検査血液学会雑誌 2017/ 鈴木敦夫ほか,医学検査 2019/ Suzuki A et al., Thromb Res 2019/ Suzuki A et al., Sci Rep 2022)
関連特許:Atsuo Suzuki, Tadasi Matsushita et al., METHOD FOR ANALYZING BLOOD SPECIMEN, AND ANALYZER. United States Patent (Patent No. US 10,739,360 B2)/ Atsuo Suzuki, Tadasi Matsushita et al., METHOD FOR ANALYZING BLOOD SPECIMEN, AND ANALYZER. European patent (Patent No. 3396384)/ 鈴木敦夫,松下正,他 血液検体の分析方法、分析装置及びコンピュータプログラム(特許第7002718号)
これまでの遺伝子解析疾患
- 血液凝固第II因子(プロトロンビン)異常症
- 血液凝固第I因子(フィブリノゲン)欠損・分子異常症
- 血液凝固第V因子欠損症
- 血液凝固第VII因子欠損症
- 血液凝固第VIII因子欠損・分子異常症(血友病A)
- 血液凝固第IX因子欠損・分子異常症(血友病B)
- 血液凝固第X因子欠損症
- 血液凝固第XI因子欠損症
- Antithrombin欠損・分子異常症
- Protein C欠損・分子異常症
- Protein S欠損・分子異常症
- Plasminogen Activator Inhibitor (PAI)-1欠損症
- Antithrombin-resistance prothrombin (ATR-FII)
- von Willebrand病
- 血液凝固第V第VIII因子合併欠損症